A ácido carboxílico es un compuesto orgánico que contiene un grupo carboxilo (C (= O) OH). La fórmula general de un ácido carboxílico es R – COOH, y R se refiere al resto de la molécula. Los ácidos carboxílicos se encuentran ampliamente. Los ejemplos importantes incluyen aminoácidos y ácido acético. La desprotonación de un grupo carboxilo produce un anión carboxilato. Los ácidos carboxílicos son una serie homóloga en la que los compuestos contienen un grupo funcional llamado grupo carboxilo (-COOH). La fórmula molecular general de los ácidos carboxílicos es CnH2n + 1COOH. Los ácidos carboxílicos contienen al menos un grupo carboxilo. Los ácidos carboxílicos con dos o más grupos carboxilo unidos se denominan ácidos dicarboxílicos, ácidos tricarboxílicos, etc.
Los ácidos carboxílicos son derivados de hidrocarburos en los que uno o más de los átomos de hidrógeno del hidrocarburo han sido reemplazados por un grupo carboxilo. Los primeros cuatro ácidos carboxílicos derivados de los alcanos son el ácido metanoico (HCOOH), el ácido etanoico (CH3COOH), el ácido propanoico (C2H5COOH) y el ácido butanoico (C3H7COOH).
Índice de contenidos
Ácido carboxílico
Ácido carboxílico, cualquiera de una clase de compuestos orgánicos en los que un átomo de carbono (C) está unido a un átomo de oxígeno (O) por un doble enlace y a un grupo hidroxilo (―OH) por un enlace sencillo. Un cuarto enlace une el átomo de carbono con un átomo de hidrógeno (H) o con algún otro grupo de combinación univalente. El grupo carboxilo (COOH) se denomina así debido al grupo carbonilo (C = O) y un grupo hidroxilo.
Los ácidos carboxílicos se identifican comúnmente por sus nombres triviales. A menudo tienen el sufijo -ic acid. También existen nombres recomendados por la IUPAC; en este sistema, los ácidos carboxílicos tienen un sufijo de ácido -oico. Por ejemplo, el ácido butírico (C3H7CO2H) es ácido butanoico según las pautas de la IUPAC. Para la nomenclatura de moléculas complejas que contienen un ácido carboxílico, el carboxilo se puede considerar en la posición uno de la cadena original incluso si hay otros sustituyentes, como el ácido 3-cloropropanoico. Alternativamente, se puede nombrar como un sustituyente “carboxi” o “ácido carboxílico” en otra estructura parental, tal como 2-carboxifurano.
 Derivados del ácido carboxílico
Derivados del ácido carboxílico
El anión carboxilato (R-COO- o RCO2-) de un ácido carboxílico se suele nombrar con el sufijo -ato, de acuerdo con el patrón general de ácido -ico y -ato para un ácido conjugado y su base conjugada, respectivamente. Por ejemplo, la base conjugada del ácido acético es acetato.
Propiedades físicas
Solubilidad
Los ácidos carboxílicos son polares. Debido a que son aceptores de enlaces de hidrógeno (el carbonilo –C = O) y donantes de enlaces de hidrógeno (el hidroxilo –OH), también participan en los enlaces de hidrógeno. Juntos, el grupo hidroxilo y carbonilo forman el grupo funcional carboxilo. Los ácidos carboxílicos suelen existir como dímeros en medios apolares debido a su tendencia a “autoasociarse”. Los ácidos carboxílicos más pequeños (1 a 5 carbonos) son solubles en agua, mientras que los ácidos carboxílicos superiores tienen una solubilidad limitada debido a la naturaleza hidrófoba creciente de la cadena de alquilo. Estos ácidos de cadena más larga tienden a ser solubles en disolventes menos polares como éteres y alcoholes.[3] El hidróxido de sodio acuoso y los ácidos carboxílicos, incluso los hidrófobos, reaccionan para producir sales de sodio solubles en agua. Por ejemplo, el ácido empático tiene baja solubilidad en agua (0,2 g / L), pero su sal de sodio es muy soluble en agua.
Puntos de ebullición
Los ácidos carboxílicos tienden a tener puntos de ebullición más altos que el agua, debido a su mayor superficie y su tendencia a formar dímeros estabilizados a través de enlaces de hidrógeno. Para que se produzca la ebullición, se deben romper los enlaces dímeros o se debe vaporizar toda la disposición del dímero, lo que aumenta significativamente la entalpía de los requisitos de vaporización.
Lista de ácidos carboxílicos
Ácidos carboxílicos saturados de cadena lineal
Átomos de carbono Nombre común Nombre IUPAC Fórmula química Ubicación o uso común
1. Ácido fórmico Ácido metanoico Picaduras de insectos HCOOH
 Ácido fórmico
Ácido fórmico
2. Ácido acético Ácido etanoico Vinagre CH3COOH
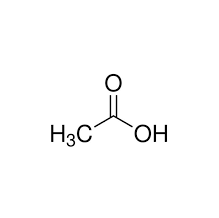 Ácido acético
Ácido acético
3. Ácido propiónico Ácido propanoico CH3CH2COOH Conservante para granos almacenados
 Ácido propiónico
Ácido propiónico
4. Ácido butírico Ácido butanoico CH3 (CH2) 2COOH Mantequilla rancia
 Ácido butírico
Ácido butírico
5. Ácido valérico Ácido pentanoico CH3 (CH2) 3COOH Valeriana
 Ácido valérico
Ácido valérico
Todas las estructuras ácidas restantes se pueden derivar como se indica arriba
6. Ácido caproico Ácido hexanoico CH3 (CH2) 4COOH Grasa de cabra
7. Ácido enantico Ácido heptanoico CH3 (CH2) 5COOH
8. Ácido caprílico Ácido octanoico CH3 (CH2) 6COOH Cocos y leche materna
9. Ácido pelargónico Ácido nonanoico CH3 (CH2) 7COOH Pelargonio
10. Ácido cáprico Ácido decanoico CH3 (CH2) 8COOH
12. Ácido láurico Ácido dodecanoico CH3 (CH2) 10COOH Aceite de coco y jabones para lavar a mano.
14. Ácido mirístico Ácido tetradecanoico CH3 (CH2) 12COOH Nuez moscada
dieciséis. Ácido palmítico Ácido hexadecanoico CH3 (CH2) 14COOH Aceite de palma
18. Ácido esteárico Ácido octadecanoico CH3 (CH2) 16COOH Chocolate, ceras, jabones y aceites
20. Ácido araquídico Ácido icosanoico CH3 (CH2) 18COOH Aceite de maní
Definición de grupo carboxilo / grupo funcional carboxilo
El grupo carboxilo es un grupo funcional orgánico que consta de un átomo de carbono con doble enlace a un átomo de oxígeno y unido de forma simple a un grupo hidroxilo. Otra forma de verlo es como un grupo carbonilo (C = O) que tiene un grupo hidroxilo (OH) unido al átomo de carbono. El grupo carboxilo se escribe comúnmente como -C (= O) OH o -COOH. Los grupos carboxilo se ionizan liberando el átomo de hidrógeno del grupo -OH. Se libera el H +, que es un protón libre. Por tanto, los grupos carboxilo son buenos ácidos. Cuando el hidrógeno sale, el átomo de oxígeno tiene una carga negativa, que comparte con el segundo átomo de oxígeno del grupo, lo que permite que el carboxilo permanezca estable incluso cuando se oxida.
El grupo carboxilo se denomina a veces grupo carboxilo, grupo funcional carboxilo o radical carboxilo. Además, podemos decir el grupo funcional de un ácido carboxílico, caracterizado por un grupo carbonilo unido a un grupo hidroxilo. El ‘carboxilo’ se puede considerar como una contracción del carbonil hidroxilo.
Un grupo carboxilo es uno de los muchos grupos funcionales que se adhiere a moléculas más grandes y les confiere ciertas propiedades. El grupo carboxilo se ve en muchas moléculas orgánicas conocidas como ácidos carboxílicos, que tienen una variedad de funciones. El grupo carboxilo consta de carbono, unido a un grupo de oxígeno e hidroxilo. Los grupos hidroxilo están simplemente unidos por oxígeno al hidrógeno.
 Grupo carboxilo
Grupo carboxilo
El oxígeno de doble enlace es electronegativo y atrae a los hidrógenos. El grupo hidroxilo hace lo contrario y con mucho gusto cedería hidrógeno para formar otro enlace con el carbono. De esta forma, los grupos carboxilo son polares y pueden participar en los enlaces de hidrógeno y en una variedad de otras reacciones importantes. La “R” en el diagrama anterior puede ser cualquier número de moléculas que contengan carbono o incluso un solo átomo de hidrógeno. Un ejemplo importante de un grupo carboxilo es la síntesis de proteínas. Cada aminoácido tiene un grupo carboxilo y un grupo amino. El enlace formado entre estos grupos permite que los aminoácidos se encadenen en secuencias largas y se conoce como enlace peptídico.
Ejemplo de grupo carboxilo
Probablemente, el ejemplo más conocido de una molécula con un grupo carboxilo es un ácido carboxílico. La fórmula general del ácido carboxílico es RC (O) OH, donde R es cualquier número de especies químicas. Los ácidos carboxílicos se encuentran en el ácido acético y los aminoácidos que se utilizan para construir proteínas. Debido a que el ion hidrógeno se desprende tan fácilmente, la molécula se encuentra más comúnmente como un anión carboxilato, R-COO–. El anión se nombra con el sufijo -ate. Por ejemplo, el ácido acético (un ácido carboxílico) se convierte en el ion acetato.
¿Para qué se utiliza el ácido carboxílico?
Los derivados del ácido carboxílico tienen diversas aplicaciones. Por ejemplo, además de su uso como desinfectante, el ácido fórmico, el ácido carboxílico más simple, se emplea en el tratamiento de textiles y como agente reductor de ácido. El ácido acético se usa ampliamente en la producción de plásticos y ésteres de celulosa.
¿Qué es un ácido carboxílico? ¿Dar un ejemplo?
Un ácido carboxílico es un compuesto orgánico que contiene un grupo carboxilo (C (= O) Oh). Los ácidos carboxílicos ocurren ampliamente. Los ejemplos importantes incluyen los aminoácidos y el ácido acético. La desprotonación de un grupo carboxilo produce un anión carboxilato.
¿Cómo se forman los ácidos carboxílicos?
La formación de ácidos carboxílicos. Como señalamos anteriormente, la oxidación de aldehídos o alcoholes primarios forma ácidos carboxílicos: en presencia de un agente oxidante, el etanol se oxida a acetaldehído, que luego se oxida a ácido acético. El ácido acético se puede oxidar aún más a dióxido de carbono y agua.
¿Qué alimentos contienen ácidos carboxílicos?
Muchos ácidos carboxílicos se encuentran naturalmente en plantas y animales. Las frutas cítricas como las naranjas y los limones contienen ácido cítrico. El ácido cítrico es un ácido carboxílico grande con tres átomos de hidrógeno ionizables. Se encuentra en las frutas cítricas y les da su sabor agrio o agrio.
¿Es el vinagre un ácido carboxílico?
El grupo funcional de los ácidos carboxílicos es el grupo carboxilo, -cooh. El vinagre es una solución diluida de ácido etanoico.
















como tiene que ver el acido carboxilico y la atraccion del zancudo y los humanos