La fórmula del nitruro de sodio se explica en este artículo. Un nitruro de metal alcalino altamente inestable, es un compuesto inorgánico. Se combinan haces atómicos de nitrógeno y sodio y se depositan sobre un sustrato de zafiro a bajas temperaturas para crearlo. Como resultado, se descompone fácilmente en sus elementos constituyentes. El nitruro de sodio tiene la fórmula molecular Na3N.
La banda prohibida es la de un semiconductor a temperatura ambiente, y casi el 90% de los átomos son iónicos. Existe una estructura anti-ReO que consiste en una celosía simple compuesta de octaedros NNa. Existe una longitud de enlace de 236,6 pm entre Na y N. Mediante difracción de rayos X, se puede determinar la conformación estructural.
Dependiendo de su proceso de síntesis, el compuesto aparece entre marrón rojizo y azul oscuro. El material no tiene punto de fusión.
Índice de contenidos
¿Qué es la fórmula química de nitruro de sodio?
Como no contiene átomos de carbono-hidrógeno, el nitruro de sodio es un compuesto inorgánico. Según su fórmula química, el nitruro de sodio contiene nitruro de metal alcalino altamente inestable. La tabla periódica coloca al sodio en el grupo 1. En este caso, los electrones se crean al perder iones 1 +, es decir, Na +, lo que resulta en electrones libres individuales.
El elemento nitrógeno pertenece al grupo 5 de la tabla periódica.
 Fórmula de nitruro de sodio
Fórmula de nitruro de sodio
Un ion nitrógeno se forma cuando se obtienen tres electrones, lo que resulta en iones N3. Para su creación se combinan átomos de nitrógeno y sodio, que se depositan sobre el zafiro a bajas temperaturas. Hay 82,976 g en una masa molecular de nitruro de sodio. Al equilibrar los iones constituyentes, se crea el componente iónico. Como resultado, tres iones de sodio se equilibran con un ion de nitruro para formar los componentes iónicos.
Na3N es la fórmula química del nitruro de sodio. Es tan inestable como el nitruro de sodio. La composición elemental del nitruro de sodio es sodio y nitrógeno, que se disuelven fácilmente entre sí.
2 Na3N → 6 Na + N2
(Fórmula de nitruro de sodio)
Es necesario calcular la fórmula de la molécula de nitruro de sodio. Los compuestos iónicos binarios se nombran de acuerdo con las siguientes reglas:
1. Los metales mantienen sus nombres y se nombran y escriben primero.
2. Ahora que la terminación del nombre no metálico es -ide, conserva su nombre base.
Los compuestos iónicos consisten típicamente en un metal (Na), que es miembro del Grupo 1A. Tiene un cargo de +1. Na + representa iones metálicos. El nitrógeno es la contraparte no metálica del nitruro. Los elementos del Grupo 5A tienen la capacidad de formar -3 iones. Entonces, N3- es el ion no metálico. Cuando la carga del ion pasa al subíndice del contraión, da lugar a compuestos iónicos. Aparecerá como Na3N en la unidad de fórmula o fórmula molecular.
Estructura del nitruro de sodio
La estructura Anti-ReO del nitruro de sodio se puede ver en su fórmula. También se encuentra una estructura de celosía simple en el nitruro de sodio, que está compuesto de octaedros NNa. Aproximadamente 236,6 pm es la longitud del enlace N-Na. La difracción de rayos X se puede utilizar para registrar la formación estructural de nitruro de sodio. Comparte el mismo anión que el nitruro de sodio con la amida de sodio y la imida de sodio. El nitruro de litio y el nitruro de potasio contienen un catión similar.
Una descripción general de la química del nitruro de sodio
- El nitrato de sodio tiene una banda prohibida igual a la de los semiconductores a su temperatura ambiente.
- El nitruro de sodio es de un color rojo azulado oscuro a marrón rojizo. Según el proceso de síntesis, los nitruros de sodio tienen diferentes colores.
- El nitruro de sodio no tiene punto de ebullición.
- Los puntos de fusión y de ebullición de los compuestos iónicos de sodio y nitrógeno son muy altos. Los iones con carga opuesta se atraen entre sí debido a la atracción electrostática.
- El nitruro de sodio se puede formar con una velocidad de entalpía de aproximadamente +64 kJ / mol.
- Los nitruros de sodio se pueden disolver en agua.
- La descomposición del nitruro de sodio tiene lugar a 86,85 ° C o 360 ° K.
Síntesis de nitruro de sodio
Por descomposición térmica de NaNH2 o por el método directo, se puede sintetizar nitrito de sodio. Se crea una cavidad cuando el sodio se forma en nitrógeno y el nitrógeno se introduce en ella como iones de sodio y se reorganizarán y se acomodarán cerca del nitrógeno. Los iones de sodio se acercan al nitrógeno para formar la banda de conducción de los electrones s. Entre ellos, hay una banda prohibida de energía, que crea un compuesto metálico que es equivalente a un semiconductor o aislante.
Conclusión
El nitruro de sodio es un compuesto inorgánico, lo que significa que no contiene enlaces carbono-hidrógeno. Los nitruros de sodio son metales alcalinos muy inestables. Como resultado, pueden descomponerse fácilmente en iones de sodio y nitrógeno. El nitruro de potasio y el nitruro de litio tienen el mismo catión que el nitruro de litio, pero son metales alcalinos que son estables. En cualquier caso, el nitruro de sodio (Na3N) se puede sintetizar por descomposición térmica de NaNH2 o por reacción directa. La conservación de alimentos se practica ampliamente con ellos.

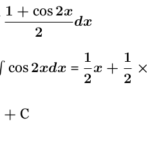












me puede ayudar con la representación de la estructura de lewis de este compuesto Na3 N