Elementos diatómicos son moléculas compuestas por solo dos átomos, del mismo o diferentes elementos químicos. El prefijo di- es de origen griego, que significa “dos”. Si una molécula diatómica consta de dos átomos del mismo elemento, como hidrógeno (H2) u oxígeno (O2), se dice que es homonuclear. De lo contrario, si una molécula diatómica consta de dos átomos diferentes, como el monóxido de carbono (CO) o el óxido nítrico (NO), se dice que la molécula es heteronuclear. El enlace en una molécula diatómica homonuclear es apolar.
Los elementos diatómicos constan de dos átomos unidos entre sí. Por el contrario, los elementos monoatómicos constan de átomos individuales. Muchos compuestos son diatómicos, como HCl, NaCl y KBr. Los compuestos diatómicos constan de dos elementos diferentes. Hay siete elementos puros que forman elementos diatómicos.
Índice de contenidos
Definición
Hay segmentos importantes que componen la atmósfera terrestre: nitrógeno, oxígeno y una pequeña muestra de argón. Para ser más precisos, el nitrógeno constituye el 78% del espacio, mientras que el oxígeno representa el 21%. Este oxígeno, O2, y nitrógeno, N2, tienen algo en común: ambos se denominan elementos diatómicos.
Como componentes puros, los elementos diatómicos son siete moléculas particulares que se componen de dos átomos. Todos los elementos de este noble grupo son gases. Si notamos el prefijo ‘di-‘ en la palabra diatómica, proviene del origen griego de ‘dos’. Una forma importante de saber que está funcionando con un elemento diatómico es considerar su fórmula. Cada molécula tiene su propia fórmula molecular única, y para los elementos diatómicos, su fórmula contiene regularmente un apéndice de 2, que realiza dos átomos en su disposición. Como ejemplo, el elemento diatómico oxígeno tiene una fórmula de O2, lo que significa que hay dos átomos de oxígeno separados presentes.
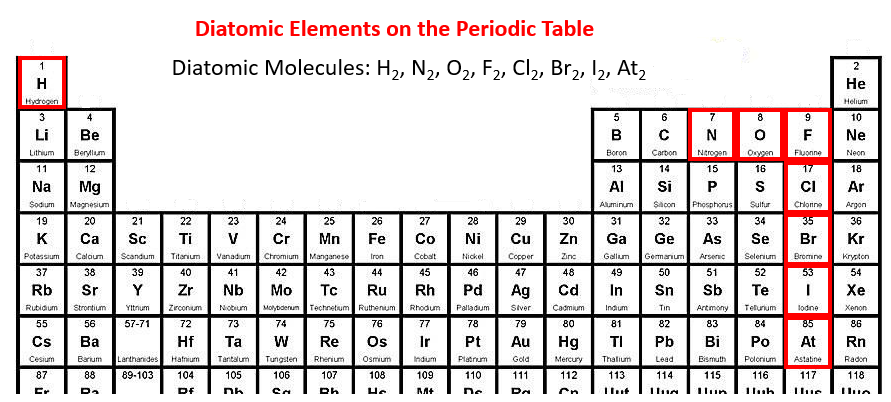 Elementos diatómicos
Elementos diatómicos
A temperatura ambiente, hay cinco elementos diatómicos, todos los cuales existen en forma gaseosa: hidrógeno, nitrógeno, oxígeno, flúor y cloro. Si la temperatura se eleva un poco más, estarán presentes dos elementos adicionales: bromo y yodo. A temperatura ambiente, el bromo y el yodo existen comúnmente en forma líquida. Sin embargo, con esa temperatura más alta, también existirán como gases.
Los elementos diatómicos son especiales ya que a los átomos que los forman no les gusta estar solos. Es decir, nunca encontrará un átomo de nitrógeno o flúor, por ejemplo, pasando el rato solo. Por el contrario, estos átomos siempre estarán emparejados porque necesitan agrupar recursos para tener suficientes electrones. Una excelente manera de recordar qué átomos forman los siete elementos diatómicos afortunados es pensar en el siguiente dispositivo mnemónico: Traigo galletas para nuestro nuevo hogar. Si alguna vez es necesario identificar estos elementos diatómicos en la tabla periódica, también se pueden detectar recordando la ‘regla de los siete’. Como se muestra en la ilustración, si toma el dedo y dibuja el número siete, comenzando por el nitrógeno, verá que seis de los elementos diatómicos están dispuestos en forma de siete. Al dibujar el número siete, no te olvides del séptimo elemento, el hidrógeno.
 Recuerde los elementos diatómicos
Recuerde los elementos diatómicos
7 elementos diatómicos
Esta es una lista de los siete elementos diatómicos. Los siete elementos diatómicos son:
- Hidrógeno (H2)
- Nitrógeno (N2)
- Oxígeno (O2)
- Flúor (F2)
- Cloro (Cl2)
- Yodo (I2)
- Bromo (Br2)
Todos estos elementos son no metales ya que los halógenos son un tipo especial de elemento no metálico. El bromo es un líquido a temperatura ambiente, mientras que los demás elementos son todos gases en condiciones normales. A medida que se baja la temperatura o se aumenta la presión, los otros elementos se convierten en líquidos diatómicos. La astatina (número atómico 85, símbolo At) y Tennessee (número atómico 117, símbolo Ts) también están en el grupo de los halógenos y pueden formar moléculas diatómicas. Sin embargo, algunos científicos predicen que Tennessee puede comportarse más como un gas noble.
Si bien solo estos siete elementos forman rutinariamente moléculas diatómicas, otros elementos pueden formarlas. Sin embargo, las moléculas diatómicas formadas por otros elementos no son muy estables, por lo que sus enlaces se rompen fácilmente.
Cómo recordar los elementos diatómicos
Hay una manera fácil de recordar el siete diatomeas, la “regla de los siete”. Primero, ve a elemento siete (nitrógeno) y luego haga un siete con el dedo a través del oxígeno y el flúor, luego baje a través del cloro, el bromo y el yodo. Eso es seis. El séptimo, el hidrógeno, es el “bicho raro” de la tabla periódica, por sí solo.
 Cómo recordar los elementos diatómicos
Cómo recordar los elementos diatómicos
¿Qué son los elementos diatómicos?
A temperatura ambiente, hay cinco elementos diatómicos, todos los cuales existen en forma de gas: hidrógeno, nitrógeno, oxígeno, flúor y cloro. Si la temperatura aumenta ligeramente, estarán presentes dos elementos adicionales: bromo y yodo.
¿Cuáles son los 7 elementos diatómicos?
Los siete elementos diatómicos son:
Hidrógeno (H2)
Nitrógeno (N2)
Oxígeno (O2)
Flúor (F2)
Cloro (Cl2)
Yodo (I2)
Bromo (Br2)
¿Son compuestos de elementos diatómicos?
Todos los compuestos son moléculas, pero no todas las moléculas son compuestos (si resulta que tienen átomos del mismo elemento). Las moléculas diatómicas son moléculas compuestas por solo dos átomos de elementos iguales o diferentes. Sin embargo, no todas las moléculas diatómicas contienen un compuesto químico.
¿Cuántos elementos diatómicos hay?
Siete elementos
Hay siete elementos que ocurren naturalmente como moléculas diatómicas homonucleares en sus estados gaseosos: hidrógeno, nitrógeno, oxígeno, flúor, cloro, bromo y yodo.
¿Es Hcl una molécula diatómica?
Todas las demás moléculas diatómicas son compuestos químicos de dos elementos diferentes. Muchos elementos pueden combinarse para formar moléculas diatómicas heteronucleares, dependiendo de la temperatura y la presión. Algunos ejemplos incluyen gases monóxido de carbono (Co), óxido nítrico (no) y cloruro de hidrógeno (HCl).